刘强医生的科普号
- 精选 SSRI类药物如何撤药
很多药物在减停过程中可发生停药综合征,以心血管及中枢神经系统药物最为常见。例如,针对14项研究的汇总分析显示,选择性5-HT再摄取抑制剂(SSRI)的停药综合征发生率平均为53.6%,且受药物半衰期、受体亲和力、治疗时长、剂量、减停方式及患者个体特征的影响。如何减停SSRI? SSRI主要通过阻断5-HT转运体发挥药理学效应。即便是短期用药,SSRI也可降低皮质5-HT2A受体及5-HT4受体密度;SSRI还可间接影响其他受体,如NE能、谷氨酸能及GABA能受体等,这些受体也可能在SSRI相关停药症状中扮演着角色。证据显示,减停SSRI可造成中缝核5-HT1A受体刺激的降低,而该受体与晕动病的发生有关;此时,患者即可能出现头晕、眩晕、恶心及疲乏等停药症状。与苯二氮类似,基于5-HT转运体占有率减药可能更为合理。需要注意的是,在SSRI有效剂量之下,5-HT转运体占有率的下降速度很快,线性减量可能造成严重的停药症状。以西酞普兰20mg为例,若以每周5mg的速度匀速减量:▲ 从20mg减至15mg时,转运体占有率下降3%;▲ 从15mg减至10mg时,转运体占有率下降6%;▲ 从10mg减至5mg时,转运体占有率下降13%;▲ 从5mg减至0时,转运体占有率下降58%。从2.5mg减至0,转运体占有率下降42.9%;即便从1.25mg减至0,转运体占有率也会下降28%,这一幅度甚至大于从40mg直接减量至5mg(27.3%)。临床中,很多患者在减停最后一点儿药物时常遇到很大的困难,也可能与上述现象有关。 为制造药理学效应上的线性下降,同样建议按比例(如10%)降低SSRI剂量,而非线性减量。对于西酞普兰而言,基于5-HT转运体占有率匀速下降10%的减量方案为:20mg,9.1mg,5.4mg,3.4mg,2.3mg,1.5mg,0.8mg,0.4mg及0mg。在国外,一些SSRI拥有液体剂型,或可解决剂量过低、药片难以分割的问题。 其他一些因素可能影响SSRI的减量过程。例如,帕罗西汀和氟西汀均经由P450 2D6代谢,进而可以抑制自身代谢,呈现非线性药代动力学。氟西汀半衰期较长,这一现象可能不具有临床意义,但对于帕罗西汀而言可能有意义。此外,帕罗西汀还具有一定的抗毒蕈碱型胆碱能受体效应及NE转运体抑制作用,也可能造成更严重的停药综合征。 而言之,尽管很多患者可以“大刀阔斧”地减停SSRI,但对于另一些患者而言,2-4周内减停SSRI可能并不够,而基于药物作用靶点占有率的更缓慢的减量或许相对稳妥,有助于减轻患者的痛苦,以及避免重新用药的波折。文献索引:Horowitz MA, Taylor D. Tapering of SSRI treatment to mitigate withdrawal symptoms. Lancet Psychiatry. 2019 Mar 5. pii: S2215-0366(19)30032-X. doi: 10.1016/S2215-0366(19)30032-X. [Epub ahead of print]
刘强 副主任医师 上海市精神卫生中心 精神科6397人已读 - 精选 AJP:抗抑郁药/认知行为疗法序贯抗抑郁的疗效
目前,抗抑郁药及心理治疗(如认知行为治疗[CBT])均为抑郁症的一线治疗手段。然而,相当一部分患者在单一初始治疗后未能获得治愈,进而需要联用其他的治疗方式。既往研究显示,对于单用抗抑郁药未能治愈的患者,联用心理治疗可有效改善残留靶症状及预防复发,改善治疗转归。然而另一方面,对于单用CBT未能治愈的患者,联用抗抑郁药的效果如何,现有证据仍相当有限。此外,在抗抑郁药的基础上联用认知行为治疗,以及在认知行为治疗的基础上联用抗抑郁药,两种序贯治疗的顺序是否影响患者的治愈率,以及联合治疗转归的预测因素有哪些,同样有待进一步探讨。PReDICT研究的第二阶段是首项比较抗抑郁药联合CBT及CBT联合抗抑郁药针对未治愈抑郁症患者疗效的大规模研究。该研究主要得到了以下结果:1.对于抗抑郁药治疗后未获得治愈的患者,联用CBT是有效的,这一点与既往研究结果一致。2.对于CBT治疗后无效或未获得痊愈的患者,联用抗抑郁药是有效的。3.无论患者首先接受的是抗抑郁药还是CBT治疗,24周时的治疗转归无显著差异。4.在预防复燃/复发方面,抗抑郁药联合CBT的效果均较好,无论采用的是何种序贯顺序。5.患者对药物或心理治疗的偏好似乎不影响联合治疗的转归。6.控制抑郁严重度因素后,焦虑可预测联合治疗后未能治愈,提示须关注及干预抑郁患者的焦虑症状。综合考虑其他研究结果,药物及心理治疗针对抑郁的疗效在很大程度上是互相独立的;联用作用机制或对脑活动模式效应不同的治疗手段,以优化治疗转归,似乎是合理的。单一治疗效果欠佳时,有必要考虑联用另一种治疗方式,顺序似乎并不重要文献索引:Dunlop BW,LoParo D,Kinkead B,et al.Benefits of Sequentially Adding Cognitive-Behavioral Therapy or Antidepressant Medication for Adults With Nonremitting Depression.Am J Psychiatry.2019 Feb 15:appiajp201818091075.doi:10.1176/appi.ajp.2018.18091075.[Epub ahead of print]
刘强 副主任医师 上海市精神卫生中心 精神科2430人已读 - 精选 如何减停苯二氮䓬类药物
苯二氮类药物(俗称安定类药物)是全球范围内最常使用的处方药种类之一,很多患者存在减停此类药物非常困难的情况,所以人们会对使用安定类药物非常恐惧,担心停不掉,俗称成瘾。当然实际情况也并非如此,很多人在专业医生指导下都很好的治愈病停药,但是有些患者因为本身使用这类药就不是在专家指导下进行,所以在碰到停药的问题后,因为缺少指导,确实会碰到很多问题,造成心理和生理上的恐惧。这里将会介绍针对减药和停药特别困难的患者可以使用的方法。当然,目前停用苯二氮尚无金标准式的减停流程。即便减停过程很小心,也无法保证万无一失。停药前,首先应认真评估患者的病史,包括苯二氮的类型(短效 vs. 长效)、剂量、使用频率、使用时长;躯体及精神共病;既往停药症状史;心理社会因素,如生活方式及人格特点。此外,还应评估患者能否在门诊安全减停,或者是否需要在住院环境下进行。为期数周至数月的减停过程更容易成功,但同样因人而异。为了尽可能提高减停成功率,减量速度不应超过每周25%。对于具体患者而言,可以考虑:▲ 在4-8周的时间内,每2周减量10%-25%。▲ 对于已经出现生理依赖的患者,可以考虑在2-12个月的时间内,每1-2周减量1/10至1/8。▲ 一些指南建议,可以将目前所使用的苯二氮换为等效剂量的地西泮(半衰期较长),随后每2周减量1/8。基于文献,使用长效苯二氮减停短效苯二氮存在不确定性,但临床基本接受这一做法。联用其他药物辅助减停苯二氮,目前尚缺乏确切证据。非药物干预联合非药物干预时,患者更容易成功减停苯二氮。为帮助患者迎接停药过程中的挑战,医生可以:▲ 确认患者的顾虑并加以安抚,表示你会为减停苯二氮给予支持,并提供其他可能有用的资源。▲ 围绕减停方案及可能出现的停药症状进行宣教,而不要让患者在缺乏信息的情况下独自前行。▲ 为患者推荐其他治疗手段,如认知行为治疗或动机式干预,以发展及强化应对技能;很多患者并不知道有这些治疗能帮到他们。▲ 设法争取患者家人及朋友的帮助,共同支持及鼓励患者完成减停。尽管一些医生对减停苯二氮的难度心存畏惧,但通过个体化的减停方案,70%-90%的患者可以成功停用苯二氮。关键在于,即便已经成功停药,这一过程中使用的某些干预手段(如认知行为治疗)也能够为患者持续带来获益。信源:Rebecca A. Payne. Kaustubh G. Joshi. Helping patients through a benzodiazepine taper. Current Psychiatry. 2019 March;18(3):9-10
刘强 副主任医师 上海市精神卫生中心 精神科3011人已读 - 精选 苯二氮䓬很容易成瘾?可能并非如此
一项针对美国患者使用苯二氮类药物(俗称安定类药物)的全国性样本的研究显示,尽管苯二氮类药物临床应用广泛,但真正达到依赖及滥用标准的个体很少:每67名使用苯二氮的美国成年人中,只有1人真正满足使用障碍的诊断标准。此外,误用苯二氮的动机通常较为“单纯”,如缓解压力、助眠、改善心境等;如果能改进这些方面的治疗,误用苯二氮的现象有望显著减少。苯二氮误用及使用障碍的相关因素包括:相对年轻,男性,黑人,受教育程度低,无医保及无业,单身,家庭收入低、合并其他物质使用问题等。苯二氮类药物常用于短期治疗焦虑及失眠。遵医嘱使用时,此类药物起效快速,疗效确切,且总体耐受性良好。然而,苯二氮误用(misuse)也并不鲜见,包括在无处方的情况下用药,使用剂量、频率、时长超出医嘱,以及用于处方之外的用途;此外,还有少数患者满足苯二氮使用障碍的诊断标准,表现为依赖及滥用,不仅造成了一系列不良转归,也加深了医生及患者对此类药物的疑虑。对专业人员而言,本项研究的结果有助于描述苯二氮使用、误用及使用障碍者的特征,早期识别误用及使用障碍的高危人群,以指导临床诊疗及预防工作。对公众而言,上述结果有助于理性看待苯二氮类药物——遵医嘱合理使用的情况下,“安定类药物”并非洪水猛兽。文献索引:Blanco C, Han B, Jones CM, et al. Prevalence and Correlates of Benzodiazepine Use, Misuse, and Use Disorders Among Adults in the United States. J Clin Psychiatry 2018;79(6):18m12174. 10.4088/JCP.18m12174
刘强 副主任医师 上海市精神卫生中心 精神科2479人已读 - 精选 焦虑性抑郁:重视苯二氮䓬的价值
众所周知,苯二氮类药物(俗称安定类药物)可有效改善焦虑及失眠症状。事实上,此类药物也具有潜在的抗抑郁活性:上世纪八十年代至九十年代早期,苯二氮的抗抑郁效应得到了相当广泛的研究。造成这一现象的原因有很多,包括当时抗抑郁药(三环类抗抑郁药[TCAs]及单胺氧化酶抑制剂[MAOIs])的副作用较多,起效速度不尽如人意,以及治疗无效率较高等。临床中,苯二氮也常用于抑郁患者,但通常并非单用或主力药物,而是作为配角与抗抑郁药联用,以改善患者原本就有或开始抗抑郁治疗后出现的焦虑和失眠症状。然而,一些研究者认为,某些苯二氮类药物,如阿普唑仑,自身或许即可治疗轻中度抑郁;虽然疗效可能不如TCAs治疗内源性抑郁患者时那样突出,但仍有望成为抗抑郁药存在使用禁忌、无法耐受或治疗无效患者的替代治疗手段。多项早期研究显示,苯二氮可用于焦虑性抑郁的治疗,但这些证据并未得到充分的分析、总结及推广营销。随着1987年氟西汀的上市,以及1992年帕罗西汀和舍曲林的上市,针对苯二氮的研究兴趣逐渐消退。数年间,SSRIs获批治疗多种焦虑障碍,在抑郁和焦虑领域都进行了大量的推广,且往往会踩在苯二氮的头上,如宣传SSRIs“不具有成瘾潜力”。另一方面,苯二氮的形象则一落千丈,被描述为疗效不及SSRIs,而且还有很强的滥用潜力。然而回过头看,“SSRIs全面优于苯二氮”的观点并没有足够的证据加以支撑:▲ Berney等在一项系统综述中得到结论:由于缺乏高质量的对比数据,焦虑障碍患者应使用新型抗抑郁药而非苯二氮的观点不一定成立。▲ 5年后,Offidani等开展的一项系统综述及meta分析显示,治疗多种焦虑障碍时,苯二氮的疗效及耐受性均优于TCAs。▲ 数项研究显示,与新型抗抑郁药如帕罗西汀或文拉法辛比较时,苯二氮组的症状改善并不落下风甚至更优,副作用也更少。与Berney等观点类似,Offidani等认为,临床更倾向于使用新型抗抑郁药而非苯二氮治疗焦虑障碍,其实缺乏支持性证据。就苯二氮类药物的一大命门——滥用潜力而言,美国精神医学学会(APA)苯二氮依赖工作组的结论是:苯二氮本身并不具有很强的推动自身使用的潜力,也并未被广泛滥用。即便苯二氮滥用真的发生了,也几乎总是发生在其他物质滥用的背景之下。然而,工作组也明确指出,长期使用苯二氮会导致生理依赖及停药症状,因此需要合理使用,包括不使用极高的剂量,以及需要在医疗监督下使用。“有成瘾潜力”并不等于“一定成瘾”;通过恰当的用药管理,风险是可控的。然而,科学的论述终究难敌风险的扩大化。苯二氮已经被贴上了“有问题”的标签,能不用则不用,这也成为了很多精神科医师的基本原则之一。焦虑性抑郁:苯二氮疗效如何?最近,Benasi等发表了一项系统综述,共纳入38项获得发表的随机对照研究,对苯二氮、抗抑郁药及安慰剂单药治疗抑郁障碍的疗效及耐受性进行了比较,研究发表于精神科期刊新贵Psychother Psychosom.。本文作者也参与了该研究。研究受试者均为非焦虑性或焦虑性抑郁患者,大部分研究使用的苯二氮为阿普唑仑(其他包括溴西泮、劳拉西泮等),抗抑郁药主要为丙米嗪及阿米替林(其他包括多塞平、氟伏沙明[唯一一种新型抗抑郁药]等)。总体而言,超过半数的研究显示苯二氮的疗效显著优于安慰剂,与TCAs相当;11项研究显示,TCAs的疗效优于苯二氮;1项研究显示,苯二氮的疗效优于TCAs。12项研究显示,苯二氮的起效速度快于TCAs。并且,绝大部分副作用在TCAs组更常见,只有困倦和认知损害在苯二氮组更常见。纳入22项研究的meta分析显示,抗抑郁药与苯二氮治疗抑郁障碍的有效率无显著差异。其中,焦虑性抑郁患者对两类药物的反应均相对较差,而抗抑郁药并不显著优于苯二氮。总而言之,尽管名字中带有「抗抑郁」,但没有证据显示抗抑郁药在治疗焦虑性抑郁患者时优于苯二氮,而苯二氮可视为与抗抑郁药平起平坐的治疗选择。值得注意的是,针对一些研究的次级分析显示,治疗药物与抑郁患者亚组存在显著的交互作用,提示临床特征不同的抑郁患者可能更适合不同类型的药物。例如,针对抑郁较轻、焦虑较重的焦虑性抑郁患者,苯二氮相比于抗抑郁药甚至具有优势。然而需要指出的是,直接比较苯二氮与新型抗抑郁药治疗焦虑性抑郁的研究几乎没有。一项为期6周、纳入112名患者的随机双盲对照研究比较了氟伏沙明与劳拉西疗抑郁焦虑混合状态的疗效,结果显示,两种药物的疗效在任何观测点上均无显著差异;副作用方面,劳拉西泮更容易导致镇静,而氟伏沙明更容易导致恶心和呕吐。我们无疑需要开展更多的类似研究,以指导临床实践。临床建议:重视焦虑焦虑是抗抑郁治疗中一个重要的“拦路虎”。然而,我们并没有对抑郁患者的焦虑及相关问题给予足够的重视;焦虑甚至不是DSM抑郁症诊断标准中的条目,只有DSM-5为抑郁症及恶劣心境增加了一个“伴焦虑特征”的标注,而针对这个标注的描述也没有出现“焦虑”的字眼。临床中往往很难区分患者的焦虑究竟是抑郁障碍症状的一部分,还是共病的焦虑障碍。不单单是抑郁和焦虑,本文作者在此前的一篇文章中已指出,精神科的共病一直是一笔糊涂账。然而很明确的是,患者同时存在抑郁和焦虑症状的比例很高。Kessler等开展的研究显示,曾罹患抑郁症的个体中,有45.7%共病至少一种焦虑障碍;STAR*D研究的第一阶段治疗中,53.2%的患者伴有显著的焦虑症状。Kessler等还提出了一个问题,即焦虑障碍与日后罹患抑郁障碍的关系。焦虑障碍可能是抑郁症起病的高危因素,以及抑郁症迁延不愈的原因。上述发现强调,我们需要充分关注抑郁患者(尤其是新近被诊断者)的焦虑问题,并针对焦虑性抑郁开展更强力的治疗。STAR*D研究第一阶段,焦虑性抑郁患者对西酞普兰治疗的反应即显著劣于无显著焦虑者,起效所需时间也显著更长。不仅疗效不好,焦虑性抑郁患者的副作用发生率也更高,严重度及负担同样更甚。第二阶段,未获治愈或无法耐受的患者换用安非他酮、舍曲林或文拉法辛,或在西酞普兰的基础上使用安非他酮或丁螺环酮增效治疗;结果显示,无论换药还是增效治疗,焦虑性抑郁患者的临床改善均更差。事实上,如果在研究中增加苯二氮的治疗选项,如第一阶段使用苯二氮治疗,第二阶段可以换用苯二氮或使用苯二氮增效,患者的状况会不会更好,尤其是考虑到很多抗抑郁药存在各种各样的副作用及停药症状。例如,很多患者难以耐受的抗抑郁药早期副作用,如恶心、呕吐、失眠及焦虑的一过性加重等,使用苯二氮时的发生率反而较低。然而,苯二氮的确可能在某些患者中造成严重的停药症状,包括焦虑、反跳性失眠甚至癫痫发作。因此,与其他一些药物(如类固醇激素、抗凝药等)一样,减停苯二氮时务必谨慎,不宜操之过急。此外,苯二氮过量死亡的个案也有报告,而FDA也强力反对联用苯二氮及阿片类药物,临床中均需注意。结语临床中,抗抑郁药联用苯二氮的情况很常见。然而,Benasi等开展的系统综述和meta分析显示,针对一类常见的抑郁患者——焦虑性抑郁,苯二氮单药治疗的效果与抗抑郁药相当,且可能起效更快,耐受性更好。在充分评估和管理苯二氮治疗风险的前提下,此类药物有望为我们所科学使用,更快、更好地缓解伴显著焦虑症状的抑郁患者的痛苦。然而,我们也需要更多的比较苯二氮与新型抗抑郁药治疗焦虑性抑郁疗效的高质量头对头研究。文献索引:Richard Balon. Benzodiazepines for anxious depression. Current Psychiatry. 2018 August;17(8):9-12
刘强 副主任医师 上海市精神卫生中心 精神科3218人已读 - 精选 围绝经期抑郁:被轻视的精神障碍
围绝经期内,女性体内激素水平剧烈波动,很容易受到一系列精神障碍的困扰,包括抑郁。很多患者、患者家属甚至医务工作者认为,围绝经期抑郁具有鲜明的年龄特色,发病原因也相对明确,本质上并不严重,挺过这段时间就好了。然而,事实是否真的如此?在这一背景下,澳大利亚莫纳什大学精神科教授Jayashri Kulkarni发表综述,对围绝经期抑郁的流行病学、诊断及治疗进行了简要回顾,旨在提醒广大医务工作者:围绝经期抑郁并非小事,临床中应加以重视,并开展个体化的干预。 流行病学: 澳大利亚本国的统计数据显示,2015年该国女性自杀率最高的年龄段为45-49岁,其次为50-54岁。将这两个年龄段连在一起考虑,我们需要认识到,与围绝经期相关的生物学改变,以及中年女性所面临的社会及心理应激,可能是导致上述年龄段女性自杀率最高的原因。 即便不考虑年龄因素,相比于男性,女性本身即承受着更重的精神疾病及自杀负担。同样是来自澳大利亚的调查数据,18-65岁女性中,有43%曾在人生的某个时点存在显著的精神健康问题。过去一年内,女性罹患心境障碍的比例为男性的2倍,罹患焦虑障碍的比例为男性的4倍;过去一年内存在精神障碍的个体中,女性存在自杀观念及计划的比例同样显著高于男性。 从社会及公共卫生角度考虑,澳大利亚健康政策协作组织曾发布文章,指出澳大利亚政府对精神卫生事业的资金支持“无效且效率低下”。该文强调,“若缺乏性别视角,数据及改革提案就会缺乏性别特异性,可能造成问题。”并且,鉴于围绝经期女性在家庭、社区及职场中往往扮演着重要的角色,抑郁焦虑所造成的社会及心理成本相当可观。 诊断 世界卫生组织(WHO)将围绝经期定义为“即将开始绝经进程,以内分泌、生物及临床改变为起始表现,至末次月经周期1年后”。因此,围绝经期抑郁的诊断常带有回顾性的特点。并且,围绝经期抑郁的“战线”往往拉得很长,患者往往首先出现心理症状,在相当长的时间(可能达到5年)后才出现躯体症状,这也增加了围绝经期抑郁的诊断难度。 医生需要意识到,女性如果在40多岁首次出现显著的抑郁或焦虑发作,即便暂无典型的围绝经期躯体症状,也应考虑到围绝经期相关激素波动导致抑郁的可能性。与之类似,若患者既往抑郁控制良好,而在40多岁时无明显诱因恶化,也应考虑围绝经期复发的可能。评估患者的抑郁是否与围绝经期有关具有临床意义,关乎后续治疗方案(如激素治疗)的合理性。 症状 围绝经期抑郁的症状范围很广,其中包括男性及年轻女性抑郁患者也经常出现的症状,但也有一些症状带有围绝经期的特点。围绝经期抑郁症状的严重度可能发生波动,时重时轻,也可能升高辨别的难度。 围绝经期抑郁的常见症状如下:▲ 精力下降▲ 偏执思维▲ 易激惹或敌意▲ 自尊下降▲ 自我隔离▲ 焦虑▲ 躯体症状(如血管舒缩症状)▲ 睡眠紊乱▲ 体重增加▲ 性欲下降▲ 记忆力受损及难以集中注意力其中,相比于男性及年轻女性抑郁症患者,认知症状、偏执及易激惹在围绝经期女性中较为突出,临床需加以注意。管理精神障碍在女性中的病程与男性存在差异,受生命周期中的生物、心理及社会学变化的影响。然而,现有大部分治疗手段主要针对“典型”的男性患者研发,对于围绝经期女性患者不一定是最优的治疗方案。针对围绝经期抑郁女性,首先应排除其他病因所致抑郁可能,如甲状腺疾病及自身免疫性疾病。上述检查也可以提供基线信息,为后续治疗做准备。排除其他原因所致抑郁可能后,围绝经期抑郁的治疗需要在生物-心理-社会模式下进行。非药物干预如果围绝经期抑郁明显与工作或人际关系问题相关,心理治疗则可视为重要的干预手段。其他一些有用的非药物干预包括针对绝经的患者宣教、规律锻炼、正念、瑜伽及饮食建议等。针对围绝经期抑郁患者,还有一个重要的提示:尽可能避免饮酒。药物或生物学干预围绝经期抑郁的主要治疗方式包括抗抑郁药及性激素相关的治疗。两者的先后顺序与患者就诊的专科及医生擅长的领域有关。若患者在围绝经期内新发抑郁,伴有其他一些围绝经期症状,无自杀倾向,总体健康状况良好,可以考虑激素治疗,但应个体化处理。国际绝经学会曾发布相关指南建议,2016年进行了更新,临床可加以参考。抗抑郁药方面,SSRI常作为一线治疗;若治疗无效,则可考虑使用SNRI。然而,一些常用的SSRI(如氟西汀)及SNRI具有激活作用,对于存在显著失眠、易激惹及焦虑的女性患者可能造成症状的恶化。作为新型抗抑郁药,阿戈美拉汀的临床应用不及SSRI及SNRI广泛,但具有一定的镇静效应,且不良反应总体较少,可能为围绝经期女性患者带来获益。一些患者对单用抗抑郁药或激素治疗反应欠佳,进而可能需要联合治疗。尽管上述两类治疗的耐受性总体较好,但一旦联用,则需密切关注治疗过程中的副作用。结语大部分女性的围绝经期抑郁对治疗反应良好,但前提是早期重视及着手干预。关键在于,不应主观地认为围绝经期抑郁并不严重,一旦激素水平稳定下来就会“自己好”。围绝经期进程可能持续数年,不能任由患者及其家人的生活质量长期受到破坏。并且,围绝经期女性自杀的情况绝不鲜见,进一步提示了围绝经期抑郁的严重性文献索引:Jayashri Kulkarni. Perimenopausal depression –an under-recognised entity. Aust Prescr 2018;41:183–5. https://doi.org/10.18773/austprescr.2018.060
刘强 副主任医师 上海市精神卫生中心 精神科2059人已读 - 精选 Lancet :运动改善情绪证据再升级,骑自行车荣获桂冠
一项对120万美国成年人健康数据的分析显示,运动能使近一个月内精神健康较差的时间减少1.5天。在研究中涉及的各项运动中,团体运动,骑自行车和健身房运动对精神健康的影响最大。能达到最大获益的运动方案是每周运动3-5次,每次45分钟。该研究于8月8日在线发表于《柳叶刀精神病学》Lancet sychiatry。重申运动的身心获益“本研究继续向临床医生重申运动对身心健康的意义”,文章的第一作者,来自美国康涅狄格州纽黑文市耶鲁大学精神病学的助理教授,Spring Health首席科学家Adam Chekroud在Medscape医学新闻中提到:“对诸如Spring Health的大型医疗系统或医疗服务企业而言,这项研究特别重要,有助于我们了解运动这一改善精神健康的重要可调控因素,这种改善无关年龄、性别、社会经济背景或身体健康状态”。“运动与多项健康获益有关,但关于运动对精神健康影响的研究,结果不甚一致”,Chekroud强调,“研究使用小样本或非代表性样本可能是导致结果相互矛盾的原因。”“个人而言,精神状态和骑自行车频率之间密切相关”,Chekroud这样描述,“从学术角度看,运动对健康的好处不胜枚举,但是从心理角度,其实多数人尚未做好通过运动来治疗精神疾病的准备,通常更愿意先尝试其他自我缓解的方式”。探索:运动缓解精神负担“曾读过一些小规模的研究,表明运动具有抗抑郁效应,我想进一步探索关于获益最大的运动类型,以及运动时间和运动频率,此类信息在既往文献中尚未涉及”。为探讨这一问题,疾病控制和预防中心(CDC)收集了行为危险因素监测系统的调查数据,并展开分析。调查数据来自2011年至2015年期间美国50个州18岁或以上的成年个体。受试者需要回答以下问题是否曾被诊断为抑郁症或有过抑郁发作近30天内有多少天“心情不好”近一个月内是否运动过,如果有,花时间最多的是哪种运动每周或每月参加运动的次数每次运动的时间(小时或分钟)协变量包括:年龄,种族,性别,婚姻状况,收入水平,教育水平,工作状态,体质指数分类,自述健康状况,以及既往抑郁症诊断。研究共纳入1,237,194名受试者,近一个月内有精神负担或精神状况不佳的平均时间为3.36天(SD,7.7;median 0;IQR,0-2).852,068名受试者的配对分析表明,相比不运动,近期参加运动的个体每月经历精神负担的时间可降低1.49天(43.2%)(W=7.42×1010,P<2.2×1016)。对既往有抑郁症诊断和无抑郁症诊断的个体进行配对分析,结果发现,运动对曾被诊断为抑郁症的受试者影响更大。运动对精神健康的影响范围广泛,不受年龄阶段、性别、种族和家庭收入的限制。最佳运动类型所有的运动类型皆可降低精神健康负担(至少可降低11.8%),但是在运动类型上存在差异。其中流行运动、骑自行车、有氧运动和健身房运动的相关性最强(分别降低精神负担22.3%、21.6%和20.1%)。即使从事家务劳动也能带来情绪获益,可使精神状态不佳的时间减少≥9.7%(每月约0.4天)。正念导向运动(瑜伽和太极拳)与也可降低精神负担,正念导向运动的个体精神负担比不运动低22.9%,比步行低(17.4%),比从事任何其他运动低(17.8)。运动越多越好?调整所有协变量后分析发现,30至60分钟(峰值约45分钟)的运动时间能最大限度的最低精神负担,这种最佳持续时间的模式在许多运动类型中都“大体一致”,但是当运动时间超过90分钟,精神负担减少的程度较小。如果运动时间超过3小时,则可能比运动45分钟或不运动精神负担更为严重。每周运动3次-5次的个体,精神负担低于每周运动次数少于3次或多于5次者。运动获益之“惊”与“喜”令人鼓舞的是,即使是相对轻松的运动(如每周三次散步)也能改善精神状态。研究者指出,“这一点很重要,因为既往研究主要集中于相对吃力的运动,如阻力训练,而这可能是大部分人无法做到的。然而,令人惊讶的是,“运动越多越好”的理念并未真正站住脚——事实上,与从不运动的个体相比,那些运动时间过长或每月运动超过22次的个体,经历坏心情的日子似乎要更多。”迄今为止最大的研究来自英国格拉斯哥加特维尔皇家医院精神病学注册处的Gary Cooney,就这一研究发表了评论,“据我所知,这是目前为止探讨健康与锻炼/体育活动之间关系规模最大的研究”。Cooney指出,“这项研究对该领域作出的最大贡献在于突出这一领域的重要性,并鼓励进行进一步研究,以探索运动类型与某种特定精神疾病的关系”然而,他表示并不愿意“从研究中找出任何可用来指导临床医生的具体信息”,因为他“对涉及到的方法论持保留意见”,具体意见于一篇社论中有所提及,包括研究人员“将所有精神障碍合并为一个整体”,“反复强调这项研究与重度抑郁症的背景”,这意味着“把精神健康与抑郁症的概念强制互换”。Cooney表示,受试者自我报告的可靠性以及对运动的定义(即包括一系列可能不符合运动定义的活动)都值得关注,有待评估。他指出,这是“一个非常困难的研究领域,因为从本质上讲,不可能做到无视受试者偏倚”,同时,他也建议“可以通过使用经过验证的评估工具,用访谈/问卷来确诊,以及避免使用'涵盖性术语'(如精神健康,运动)来优化研究的科学性与严谨性。”Chekroud博士补充说:“展望未来,我们很高兴能够将这项研究作为个性化精神病学计划的一部分,为患者提供个性化的运动方案,以帮助他们改善精神健康。”信源:More Evidence Exercise Improves Mental Health-Medscape,August 13,2018
刘强 副主任医师 上海市精神卫生中心 精神科1785人已读 - 精选 超越单胺:未来的抗抑郁药长什么样?
自1959年丙米嗪获批上市以来,美国食品药品监督管理局(FDA)近六十年内批准的所有抗抑郁药均主要通过单胺能递质系统发挥治疗效应,包括调节突触间隙5-HT、NE、DA的浓度,和/或这些递质与突触后受体的结合。然而据保守估计,至少三分之一的患者对这些万变不离其宗的单胺能抗抑郁药反应不佳,呼唤着新型抗抑郁药的诞生。尽管很多新型抗抑郁药在临床2期或3期研究中铩羽而归,但也有一些抗抑郁药仍坚挺在不同的研究阶段,并有望进入临床,进一步充实医生的抗抑郁弹药库。目前最接近上市的药物包括N-甲基-D-天冬氨酸(NMDA)能药物,如艾氯胺酮和rapastinel;阿片受体部分激动/拮抗剂,如Alkermes 5461;GABAA受体调节剂,如别孕烯醇酮。更远一些的潜力药物包括致幻剂,如著名的裸盖菇素。NMDA能药物NMDA受体拮抗剂的前景最为人所看好。作为1970年获批上市的老牌麻醉剂,静脉给予氯胺酮在早期研究中展现出了针对难治性抑郁的不凡潜力,这也导致多家药厂一拥而上,试图研发拥有专利权的NMDA受体拮抗剂。其中,最有可能拔得头筹的是氯胺酮的一种对映异构体——艾氯胺酮(esketamine)。由于亲和力属性更优,艾氯胺酮有望经鼻给药,而无需采用有创性的静脉给药。已有研究显示,艾氯胺酮可有效改善难治性抑郁及急性自杀倾向。强生计划今年向FDA递交上述结果,以寻求获批上市。另一种有潜力的NMDA受体拮抗剂,rapastinel,也正在临床研究中披荆斩棘。然而即便上市,该药可能也需要静脉给药,进而对临床应用构成限制。回到氯胺酮。尽管氯胺酮在抗抑郁领域只有一些早期证据,但已有一些独立执业的医师及某些医疗机构开始为罹患难治性抑郁且不差钱的患者提供超说明书的氯胺酮静脉输液治疗。面对饱受困扰的抑郁患者,试图给予其帮助是可以理解的;然而,我们目前所掌握的知识仍相当有限,尤其是氯胺酮治疗抑郁的长期疗效及安全性,这一点务必加以考虑。针对氯胺酮静脉输液治疗,目前基本没有制度约束。医生和患者都应该对此类治疗的潜在风险有所了解,在治疗过程中多加小心,并关注潜在的解离副作用及滥用风险;还要知道,平均每两名难治性患者中也只有一人能够从氯胺酮治疗中获益。随着研究证据及临床经验的逐步积累,在安全应用的前提下,NMDA能药物有望为抑郁患者带来独特的疗效获益。阿片能药物阿片受体激动剂拥有一定的抗抑郁活性;问题在于,此类药物的疗效很容易出现耐受,导致患者需要使用越来越高的剂量。那么,如果联用一种阿片受体部分激动剂与一种纯粹的阿片受体拮抗剂,能否在保证安全性的情况下,无需加量即可持续收获疗效?事实上,这样的药物已经出现了:丁丙诺啡属于μ受体及κ受体部分激动剂,而samidorphan属于μ受体拮抗剂,两者所构成的复方制剂正在接受FDA的审查。尽管3期临床研究的结果尚未发表,但已经发表的2期研究显示,这一复方制剂与其他药物联用时,低剂量(丁丙诺啡2mg+samidorphan 2mg)即可有效改善难治性抑郁。多项壁报研究也显示,该药展现出了崭新的抗抑郁作用机制及较好的安全性。然而可以预见的是,该药获批上市后,向医生和公众解释其略显矛盾的作用机制将花费很大的力气,包括阿片能激动与阿片能调节/拮抗的关键差异。尤其是考虑到作用机制关乎长期使用的利弊权衡、滥用潜力及安全性等问题,这种解释工作又必须要做。GABAA受体调节剂Brexanolone是别孕烯醇酮的一种静脉制剂,属于GABAA受体正性变构调节剂。已有研究探讨了该药针对产后抑郁的疗效,并取得了阳性成果。该药的早期研发过程中,研究者将目光锁定在了“经静脉给药治疗产后抑郁”这一高度具体的课题;然而,以GABAA受体作为靶点治疗抑郁,这一新概念有望催生出更多的成果,用于治疗范围更广的难治性抑郁患者。此外,该成分的一种口服剂型SAGE-217正处于早期临床研究阶段。致幻剂在尝试获得FDA批准之前,致幻剂尤其是裸盖菇素早已名声在外,在难治性抑郁研究中崭露头角。一项小规模双盲研究显示,裸盖菇素可显著改善终末期癌症患者的抑郁和焦虑症状。另一项针对难治性抑郁患者的开放标签研究显示,使用两剂裸盖菇素后,抗抑郁获益甚至可以持续6个月之久。神经影像学研究显示,裸盖菇素可造成特定脑区静息态功能连接的改变,或可解释抑郁症状的改善。上述发现均仍处于初级阶段,但由于前景颇为光明,已经促成了数项针对致幻剂的2期随机对照研究。需要指出的是,迄今为止所有针对致幻剂的研究(包括仍在筹备中的研究)在给予治疗药物时,患者均处于控制精良、监督严格的心理支持环境下。结语以上哪些新型抗抑郁药将最终获批进入临床,目前仍不清楚。然而,如此多的新型抗抑郁机制正在接受严格的评估,并有望造福患者,仅这一点已经令人欣慰和兴奋了。信源:Aaronson ST.Beyond the monoamines:The future of antidepressants.MDedge.August 16,2018
刘强 副主任医师 上海市精神卫生中心 精神科2335人已读 - 精选 精神分裂症共病强迫的治疗
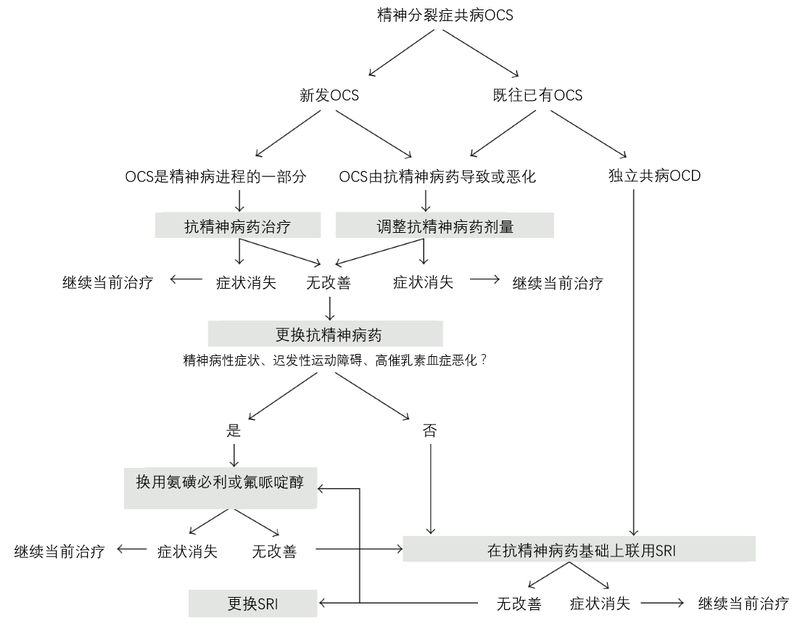
精神分裂症共病强迫症(OCD)相当常见。数据显示,约25%的精神分裂症患者存在强迫症状(OCS),其中12%满足OCD诊断标准。精神分裂症患者的OCS可出现于各个时段,包括前驱期、急性期及用药后;值得注意的是,部分抗精神病药也可诱发OCS。 针对精神分裂症与OCD的高共病率,目前存在若干种解释。例如,2014年一项发表于《美国医学会杂志·精神病学》的全国性研究显示,OCD可显著升高日后罹患精神分裂症谱系障碍的风险。另一方面,已经罹患精神分裂症的患者可能同时存在精神分裂症或OCD的易感基因,环境因素(如应激、抗精神病药等)可触发OCD基因的表达,进而造成共病。 精神分裂症共病OCD/OCS的治疗应遵循个体化原则。基于强迫症状与精神分裂症的时间关系,药物选择也有所不同。在现有抗精神病药的基础上,可考虑联用SSRIs;对于抗精神病药所致OCS,推荐使用氨磺必利。治疗流程图如下
 刘强 副主任医师 上海市精神卫生中心 精神科3823人已读
刘强 副主任医师 上海市精神卫生中心 精神科3823人已读 - 精选 2016年CANMAT成人抑郁症指南
2016年8月2日,加拿大心境和焦虑治疗网络(CANMAT)发布了成人抑郁症管理指南。该指南包括六大部分内容,分别为:1、疾病负担和护理原则;2、心理治疗;3、药物治疗;4、神经刺激疗法;5、补充和替代疗法;6、特殊人群(儿童/青少年,女性,老年人)。以下为抑郁症及其治疗的高危因素汇总:发病方面治疗方面2016年8月,加拿大情绪和焦虑治疗网络(CANMAT)发布了成人抑郁症的管理指南,该指南主要包括6大部分内容,分别为:1.疾病负担和护理原则;2.心理治疗;3.药物治疗;4.神经刺激疗法;5.补充和替代疗法;6.特殊人群(儿童/青少年,女性,老年人)。现整理药物治疗部分如下:文献索引:Lam RW, et al.Canadian Network for Mood and Anxiety Treatments (CANMAT) 2016 ClinicalGuidelines for the Management of Adults with Major Depressive Disorder:Introduction and Methods. Can J Psychiatry. 2016 Aug 2. pii: 0706743716659061.[Epub ahead of print]
刘强 副主任医师 上海市精神卫生中心 精神科5115人已读






